Cell丨闵军霞教授团队联合医学院张强研究员及王福俤教授团队,发表重磅成果:破译铁死亡“铁池双柄总阀门”,开辟重大疾病治疗新赛道
铁死亡是铁离子依赖性调控性细胞死亡,现已成为生命医学领域国际前沿与研究热点,是探索生命本质、攻克重大疾病、研发原创新药的核心突破口。细胞铁池稳态、谷胱甘肽抗氧化、脂质过氧化三大核心轴共同决定铁死亡的启动、进程与转归。围绕抗氧化与脂质过氧化通路,领域已发现GPX4、FSP1等里程碑式靶点;然而,真正居于铁死亡上游、起到决定性驱动作用的 “细胞铁池” 精密调控机制,长期未能实现关键突破,成为领域悬而未决的世界难题和“世界遗憾”。
北京时间 4 月 27 日,浙江大学医学院张强研究员团队(基础医学院)联合王福俤教授团队(公共卫生学院)、闵军霞教授团队(转化医学研究院),并携手上海中医药大学附属市中医医院巴乾研究员,在国际顶级期刊《细胞》(Cell)在线发表重磅研究成果,彻底破解这一长期悬而未决的科学难题。该研究首次发现细胞铁代谢核心调控蛋白 MARCH7,揭示其通过 “双通路总控”机制,同时抑制铁的过量摄入与异常释放,因此将 MARCH7 定义为“Ferro‑Guardian 铁卫士”,从根本上填补了铁死亡领域上游铁调控机制的核心空白。团队还原创构建 MARCH7 可视化探针,并通过高内涵筛选首次鉴定出特异性小分子稳定剂 EmodAn,在两种重大心脏疾病动物模型中展现出显著器官保护效果,为铁稳态失衡相关疾病的新药研发提供了源头创新靶点与全新策略。

浙江大学医学院21级博士生黄文祥(已毕业)、22级博士生王睿君(已毕业)、博士后杨鑫泉和杨双杰为本文共同第一作者。
协同攻坚:三位科学家共筑“铁科学”新版图
这项系统性工程的背后,是张强研究员、王福俤教授和闵军霞教授三位核心科学家的深度协同与优势互补。
作为国际铁死亡与铁代谢领域的开创者和领军人物,王福俤教授早在数年前就洞察到,铁死亡研究必须从“脂质过氧化”的单一视角转向“铁代谢调控”的全局视野,并全球首次提出“铁死亡信号”“FerroLipid铁脂调控”原创理论。“这项工作的核心科学问题,是我们大团队长期深耕的方向。”王福俤教授强调,“铁池失衡不仅仅是铁死亡的结果,更是其原始驱动因素。找到既能感知铁水平、又能双向调控铁稳态的‘总开关’,是领域最核心的科学使命,更是我们的梦想。”
闵军霞教授则从临床转化角度进行了整体设计:“我们不仅要发现新靶点,更要证明它可成药。因此,我们从课题设计之初就规划了从‘机制阐明’到‘药物筛选’,再到‘动物验证’的全链条研究路径。”
而将这一宏大科研蓝图变为现实的,是张强研究员带领的技术驱动型团队。他主导了从多组学筛选、机制解析,到荧光探针设计、高内涵药物筛选的全链条全新技术攻坚。正是依托他团队搭建的独特成像平台和系统的筛选体系,MARCH7这一全新靶点得以被发现,EmodAn得以被成功鉴定,实现从 0 到 1 的突破。王福俤教授由衷赞叹: 张强团队搭建的蛋白精准筛查与成像体系,如同穿透生命迷雾的‘科学之眼’,又如直抵核心机制的‘攻坚利剑’,让原本深藏的科学设想一一变为现实;而闵军霞教授对铁死亡本质的深刻洞察与精准把控,则如浩瀚星河中的恒久星光,指引方向、照亮前路。
正是王福俤和闵军霞两位教授对课题的顶层设计、系统实验体系支撑和科学方向的精准把控,以及在应对《细胞》期刊审稿人严苛问题时反复斟酌、补充实验的严谨态度,加之张强研究员团队精湛的技术攻坚与系统性的实验推进,才最终确保了这项里程碑式工作的顺利诞生。三位科学家紧密协作,堪称“战略科学家领航+技术科学家攻坚”协同创新的典范。


颠覆认知:发现铁死亡的“双柄总阀门”MARCH7
铁死亡的发生,依赖于细胞内铁过载所驱动的脂质过氧化。此前,科学界对铁进入细胞(通过TFR1受体)以及铁从铁蛋白储存库中释放(通过NCOA4介导的铁蛋白自噬)已有基本认识——TFR1和NCOA4堪称铁代谢调控的两员干将,但一个根本性的问题始终存在:在这两员干将之上,是否还有一位更上游的“统帅”,能够统一调度铁的流入与流出?
本研究通过多组学筛选,首次鉴定出E3泛素连接酶MARCH7是铁死亡中调控铁代谢的关键分子。进一步的深入探索中,团队逐渐明晰了MARCH7蛋白在细胞铁死亡中的精密双通路调控机制:它一方面通过泛素化降解NCOA4蛋白来螯合铁离子;另一方面泛素化TFR1蛋白并控制其空间转位来抑制铁离子的吸收,最终以一种“上游总阀门”的模式操控细胞内铁稳态。这一发现为理解细胞如何主动限制铁过载以抵御铁死亡,提供了全新的分子机制。
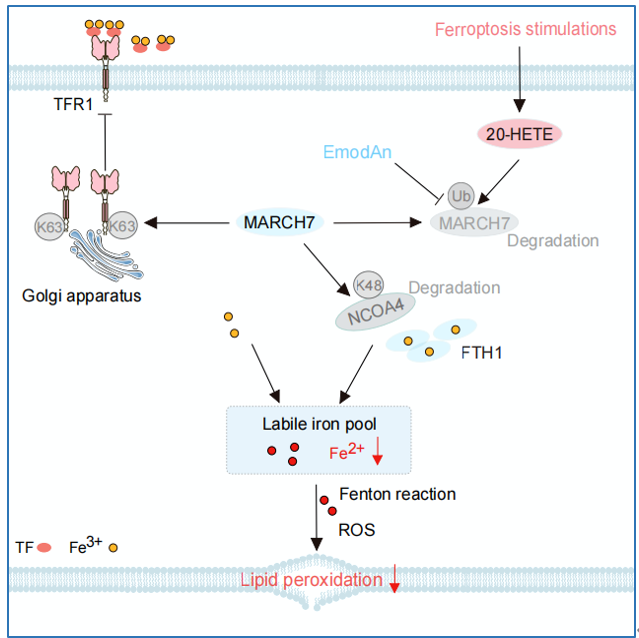
MARCH7介导铁代谢和铁死亡的机制分析
开拓蓝海:为First-in-class 原创新药提供源头核心靶点
长期以来,铁死亡领域药物研发局限于脂质过氧化下游抑制(如 Ferrostatin‑1),靶点单一、转化受限。MARCH7 的原创发现,彻底打破困局,开辟 “上游调控铁稳态、主动防御铁死亡” 全新赛道,实现研发从 “被动抑制” 到 “主动修复” 的范式革新。
“我们的研究深化了铁在铁死亡中的核心调控认知。”闵军霞教授强调,“MARCH7作为铁稳态双通路总控开关,是全新原创靶点,为 First-in-class 药物研发奠定坚实基础。”
依托该发现,团队通过高内涵筛选,从上千个天然产物中首次鉴定出特异性小分子 EmodAn,可高效稳定 MARCH7、抑制其降解。在阿霉素诱导性心肌病、心肌缺血再灌注损伤两种重大心脏疾病模型中,EmodAn 疗效显著优于Ferrostatin‑1,可显著减轻心肌损伤、降低死亡率。
这一突破证实,靶向激活内源性 “铁卫士” MARCH7,是更上游、高效、安全的干预策略,可广泛应用于铁稳态失衡相关重大疾病,为全球原创新药研发开辟全新赛道,具备重大临床转化价值。
开创未来:从“浙大铁力量”到全球引领
《Cell》的匿名评审专家对该研究给予高度评价:“我相信这些发现将引发广泛关注,将促进MARCH7在铁死亡中作用的进一步研究。”“该研究无疑为铁死亡提供了全新机制见解,作者们付出的巨大努力值得充分肯定。”
“这项研究是典型的浙大协同创新模式。” 张强研究员表示,在王福俤教授、闵军霞教授的战略布局与统筹下,技术团队充分发挥专业优势,三方深度联动、优势互补,构建起 “临床问题导向 — 基础机制阐明 — 靶点挖掘 — 药物筛选验证” 的全链条研究体系,实现了从基础研究到临床转化的无缝衔接。目前,合作团队正围绕更前沿、更系统、更具突破性的科学问题,持续推进深度协同创新。
王福俤教授指出:“这项研究的价值,远不止于发现一个新分子、揭示一套新机制,更从根本上重塑了铁死亡领域的认知格局。我们首次找到调控铁稳态失衡的上游‘总开关’——MARCH7,证实细胞可通过主动调控铁代谢、遏制铁过载来抵御铁死亡,标志着铁死亡研究正式从‘脂质单一调控’的单核驱动时代,迈入‘铁稳态调控 + 脂质调控’的双核协同时代。这一突破,必将改写全球铁死亡及相关疾病的研究范式与教科书体系。”
闵军霞教授由衷感慨:“从临床转化来看,这一突破彻底打破传统研发瓶颈,为铁稳态失衡相关疾病开辟了全新药物赛道。相较于以往被动抑制脂质过氧化,我们如今可激活细胞自身铁稳态调控能力,实现更上游、更精准、更安全的干预。团队已成功鉴定首个 MARCH7 特异性小分子稳定剂 EmodAn,并建成‘临床需求 — 分子机制 — 靶点发现 — 药物筛选 — 动物验证’的全链条创新体系。下一步,我们将全力推进临床前研究与临床试验,力争把这项原创成果转化为真正惠及患者的新药,为重大疾病防治贡献中国智慧与浙大力量。”

团队合影照片
该项研究由浙江大学医学院张强研究员、王福俤教授、闵军霞教授、上海中医药大学附属市中医医院巴乾研究员,山东博观成像生物科技有限公司吴军兵博士担任共同通讯作者。浙江大学医学院2021级博士生研究生黄文祥、2022级博士生研究生王睿君,博士后杨鑫泉和杨双杰为共同第一作者。本研究得到了南京大学医学院刘志红院士、浙江大学基础医学院徐浩新教授和浙江理工大学付彩云教授的指导支持,以及浙江凯莱普公司孔子青博士和浙江大学医学院附属第一医院博士后孟凡超的大力帮助。本研究获得了多项国家自然科学基金、上海市东方英才拔尖计划,中国博士后面上基金和浙江大学基础医学院院长基金等项目的资助。


