Nano Today丨周民团队:细胞膜修饰牙龈卟啉单胞菌用于肿瘤微环境免疫调控和光热免疫治疗
针对生物材料的设计,长期以来一直专注于惰性材料,以避免与免疫系统的相互作用,防止不利生物体的异物反应。随着对免疫系统的认识不断加深,研究人员们开始采用新的策略来调节免疫细胞和生物材料之间的相互作用。单核细胞源性巨噬细胞(Monocyte-derived macrophages, Mφ)作为重要的先天免疫细胞之一,发挥着吞噬清除和抗原提呈的重要作用。大多数恶性肿瘤高Mφ浸润,且Mφ可广泛分为M1表型和M2表型。肿瘤微环境(TME)增强M2表型以维持免疫抑制,使肿瘤生长。相反,M1巨噬细胞通过释放促炎因子来抑制肿瘤生长。因此,通过调节细胞群,重编程表型,促进M2向 M1极化,可以有效控制肿瘤生长。
近期,浙江大学周民教授课题组在国际知名期刊Nano Today上发表文章Wrapping Porphyromonas gingivalis for tumor microenvironment immunomodulation and photothermal immunotherapy,(IF=20.722)。本研究设计了一种红细胞膜涂层的牙龈卟啉单胞菌(cmPg),红细胞膜涂层改善了细菌的大小分布,减少了巨噬细胞对细菌的清除,并维持了细菌对巨噬细胞的极化作用。cmPg能够稳定产生黑色素,在激光照射下可作为光热治疗剂(PTT),促进癌细胞发生光热诱导免疫原性细胞死亡(ICD)。该免疫调节细菌与anti-PD -1联合使用,可抑制B16F10黑色素瘤和CT26结肠癌原发和继发肿瘤的生长。本研究提供了一个直接的策略,将Pg的角色从炎症细菌转变为预防癌症的生物材料。通过使用生物工程方法将光热治疗、细菌治疗和anti-PD-1免疫治疗相结合,其生产工艺并不复杂,机理明确,便于后期开展临床转化研究。
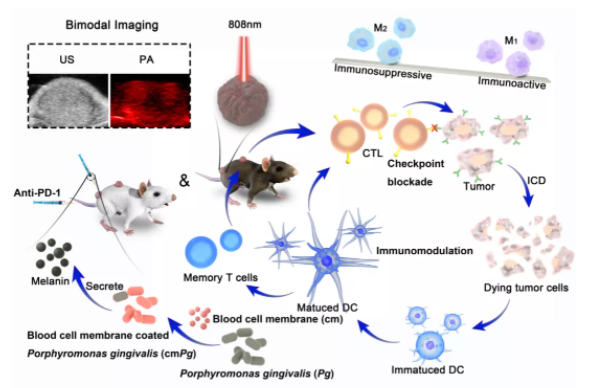
实验证明了细菌炎症反应与抗肿瘤反应可以有效结合。cmPg含有CD47蛋白,能够逃脱巨噬细胞的吞噬,以较少的细菌数量释放更多的黑色素。在照射后,cmPg可实现黑色素光热转换,并能迅速提高温度,提高US/PA成像信号强度。在细胞和组织中发现了CD206、CD80、IL-6、IL-12、IL-10和MCP-1的表达,说明了cmPg的调控行为。该联合治疗策略包括三部分:cmPg、激光治疗和anti-PD -1检查点阻断,在延长生存率方面有明显改善。此策略能激活免疫系统,促进成熟树突状细胞、细胞毒性淋巴细胞、记忆T细胞和抗肿瘤M1型巨噬细胞的增加。
浙江大学转化医学研究院博士后陈琪是论文的第一作者,浙江大学周民研究员和王凯教授是论文的通讯作者。上述研究工作得到了国家自然科学基金和中国博士后科学基金的资助,浙江大学癌症中心以及现代光学仪器国家重点实验室的大力支持。
论文链接:
https://www.sciencedirect.com/science/article/pii/S174801322100236X


