Nature Communications丨吕志民教授团队发现葡萄糖激酶调控Hippo-TAZ通路促肿瘤生长
近年来吕志民教授团队研究发现,多种代谢酶具有“兼职”功能。某些代谢酶可发挥蛋白激酶活性,参与调控信号转导和基因表达等。这一发现为理解细胞生命活动的复杂调控机制提供了全新视角。由于代谢酶的双重功能在肿瘤中扮演关键角色,针对其激酶活性的抑制剂可能成为新型治疗策略。探索代谢酶如何在不同环境下切换“代谢酶-蛋白激酶”模式,将有助于揭示更广泛的细胞调控网络,为疾病治疗提供新的靶点。
2025年8月4日,浙江大学转化医学院/浙江大学医学院附属第一医院/国家基础科学中心吕志民、青岛大学肿瘤研究院方靖和青岛大学附属医院邱文生等在Nature Communications上发表了题为“Nucleus-translocated glucokinase functions as a protein kinase to phosphorylate TAZ and promote tumour growth”的研究论文,报道了缺氧条件会诱导葡萄糖激酶(GCK)发生核转位,通过磷酸化Hippo通路关键效应分子TAZ驱动肿瘤进展。该研究揭示了肿瘤细胞在缺氧环境下通过重塑细胞关键信号通路实现适应性生长的重要分子机制,为理解肿瘤代谢与信号通路的交互作用提供了新的视角。

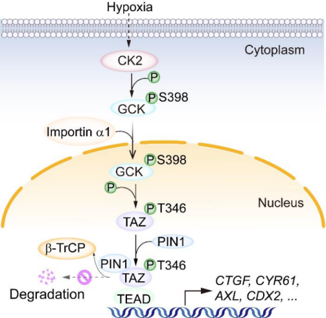
研究发现,在缺氧环境中,肿瘤细胞中的酪蛋白激酶2(CK2)会磷酸化GCK的第398位丝氨酸,使GCK暴露出核定位信号,进而与转运蛋白importin α1结合并转移至细胞核。令人意外的是,传统认知中参与糖代谢的GCK在核内展现出新的功能-作为蛋白激酶直接磷酸化转录共激活因子TAZ的第346位苏氨酸。磷酸化的TAZ会招募肽酰脯氨酰异构酶PIN1,通过构象变化阻止β-TrCP泛素连接酶对TAZ的识别,从而抑制TAZ的降解。稳定的TAZ随后与转录因子TEAD形成复合物,激活细胞增殖、存活等基因表达,最终促进肿瘤生长。这一发现阐明了GCK在缺氧条件下对Hippo通路的直接调控作用,为肿瘤治疗提供了新思路。
原文链接:https://www.nature.com/articles/s41467-025-62566-4


